Tendencias Generales De La Tabla Periodica
Recuerde que estas tendencias se basan en variaciones periódicas en una sola propiedad fundamental la carga nuclear efectiva Z eff que aumenta de izquierda a derecha y de arriba a abajo en la periódica mesa.
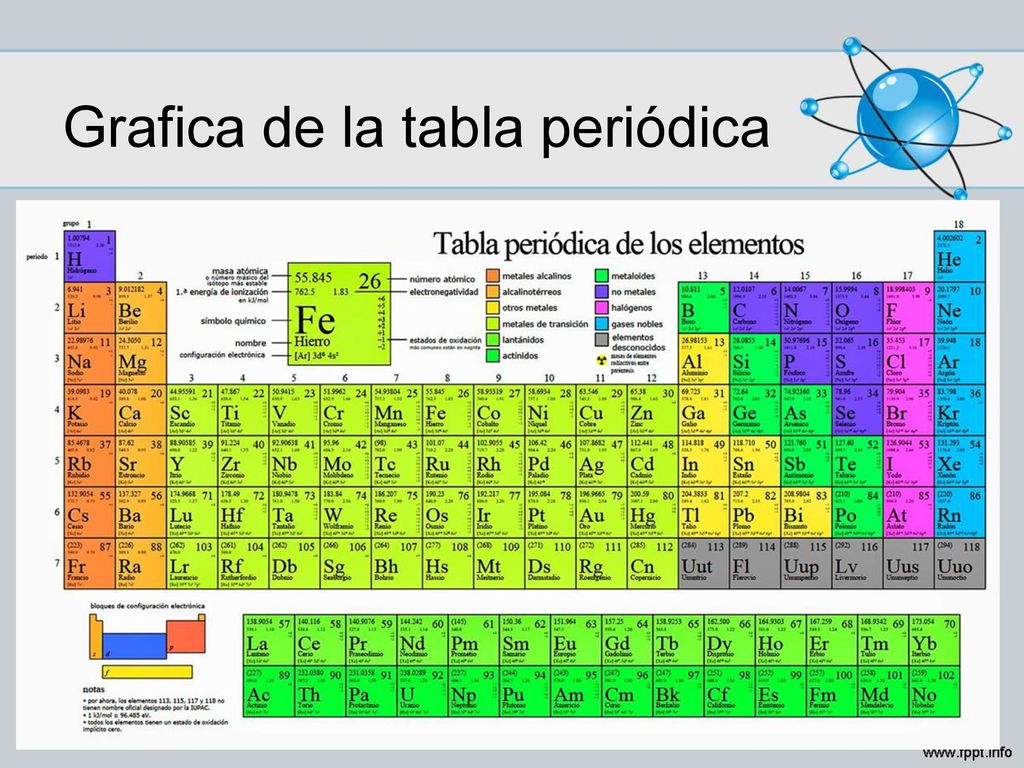
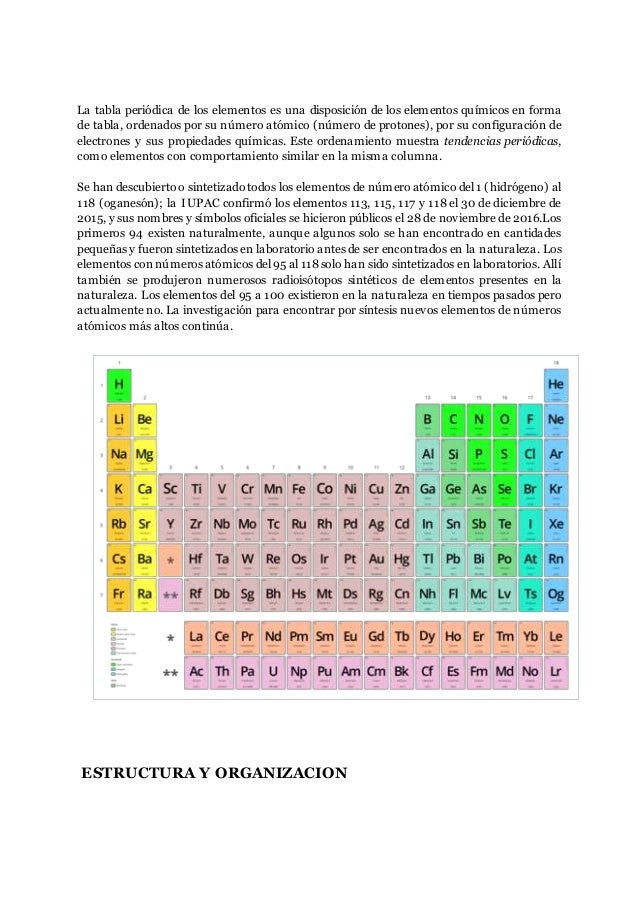
Tendencias generales de la tabla periodica. - Existen dieciocho grupos. Tendencias en la tabla periódica. Las propiedades de los elementos son funciones periódicas de sus números atómicosLa tabla periódica incluye todos los elementos conocidos 118 ubicados en orden.
Se llaman periódicas porque se repiten en la tabla periódica. Tendencia en los periodos. Tendencias en Radio atomico.
Las afinidades electrónicas no cambian mucho al bajar en una familia. Propiedades de ácidobase de óxidos en un período de. No tiene un lugar fijo para el hidrógeno.
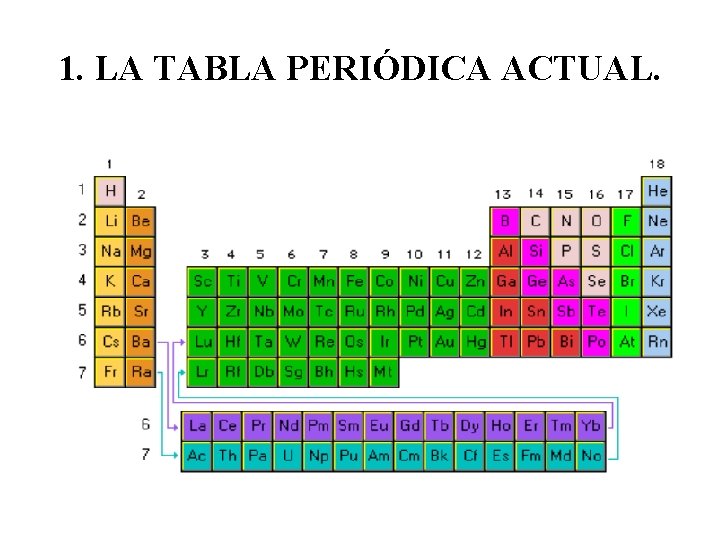
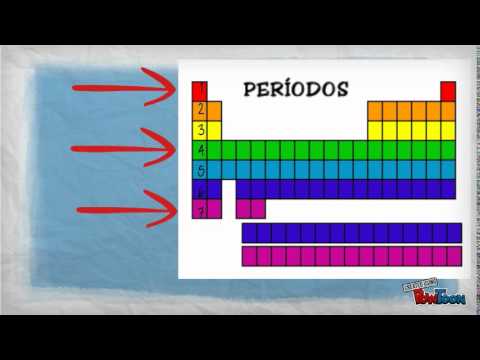
Carácter de propiedades y metálicos no-metálico de redox. La tabla periódica cuenta con 7 períodos y los elementos pertenecientes a un mismo periodo presentan tendencias similares de electronegatividad afinidad electrónica ionización y radio atómico. - Los elementos situados en dos filas fuera de la tabla son del grupo 3.
Primera y segunda energía de ionización. Las tendencias periódicas son patrones específicos que están presentes en la tabla periódica que ilustran diferentes aspectos de un determinado elemento incluido su tamaño y sus propiedades electrónicas. Caracteristicas generales de la tabla periodica Características generales de las familias de la tabla periódica Hay 18 grupos los cuales son.
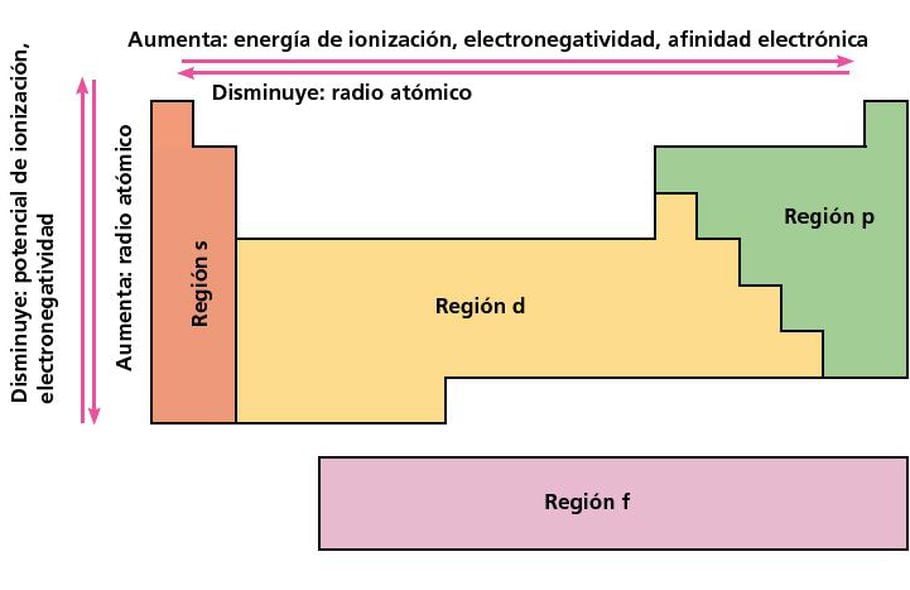
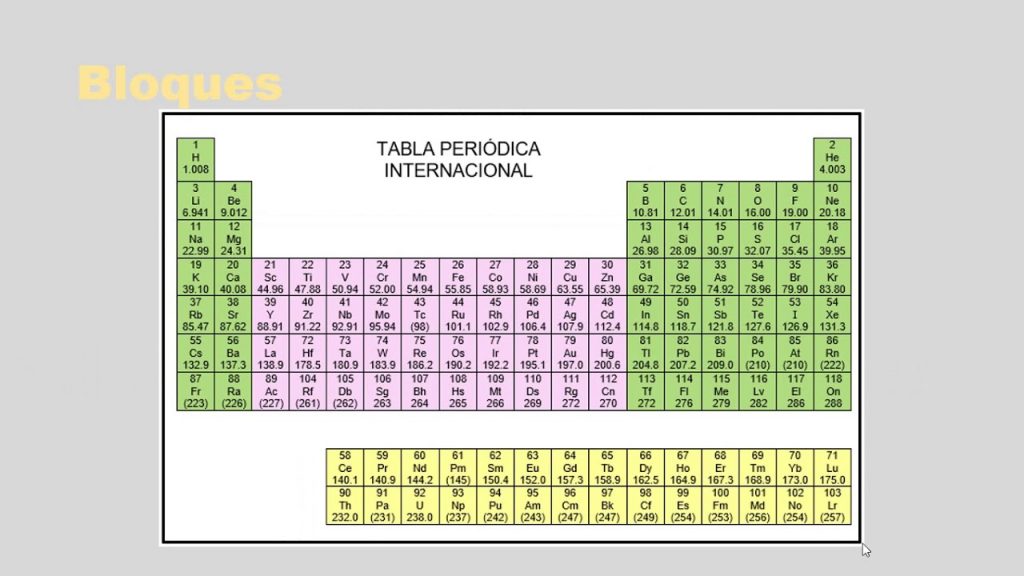
Se estructura en bloques. Esto ocurre debido a que los elementos coinciden en la configuración electrónica en el último nivel. Los elementos se agrupan de acuerdo con una estructura electrónica similar lo que hace que estas propiedades recurrentes.
Todos estos tienen un electrón en su último nivel energético mas extremo contundencia a desaparecer - Grupo 2IIA. Tendencias del radio atómico en la tabla periódica. Los metales alcalinos litio sodio potasio rubidio cesio francio.
Generalidades de la tabla periódica Clasificación periódica de los elementos Su función principal es establecer un orden específico agrupando elementos. Las propiedades químicas de los elementos dependen de la distribución electrónica en los diferentes niveles por ello. Mini video sobre el tamaño de los iones.
Defectos de la tabla de Mendelejeff. Resumen de las tendencias en la tabla periódica. Al final del siglo se determinó que la valencia coincidía con el número de electrones que gana cede o comparte un átomo de un elemento al formar una unión en una sustancia químicaLa Ley Periódica se enuncia de esta manera.
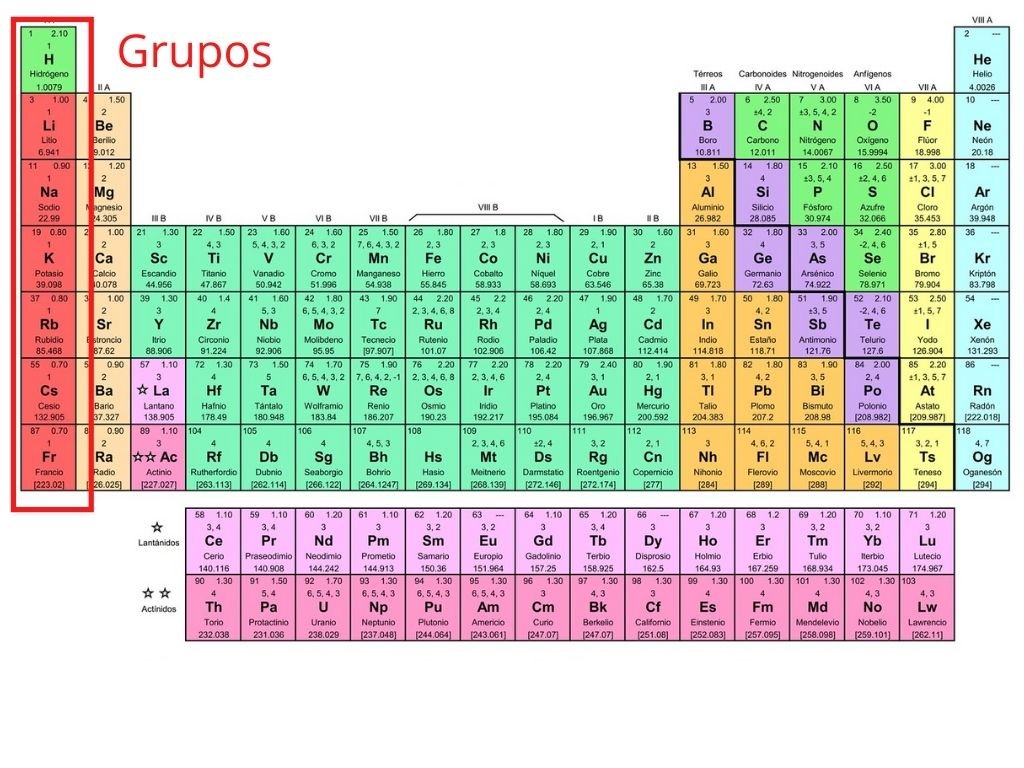
Radio atómica energía de ionización. Periodos Grupos - Las columnas de la tabla reciben el nombre de grupos. El conjunto de elementos con el nombre de tierras raras o escasas lantánidos no tiene ubicación en la tabla o es necesario ponerlos todos juntos en un mismo.
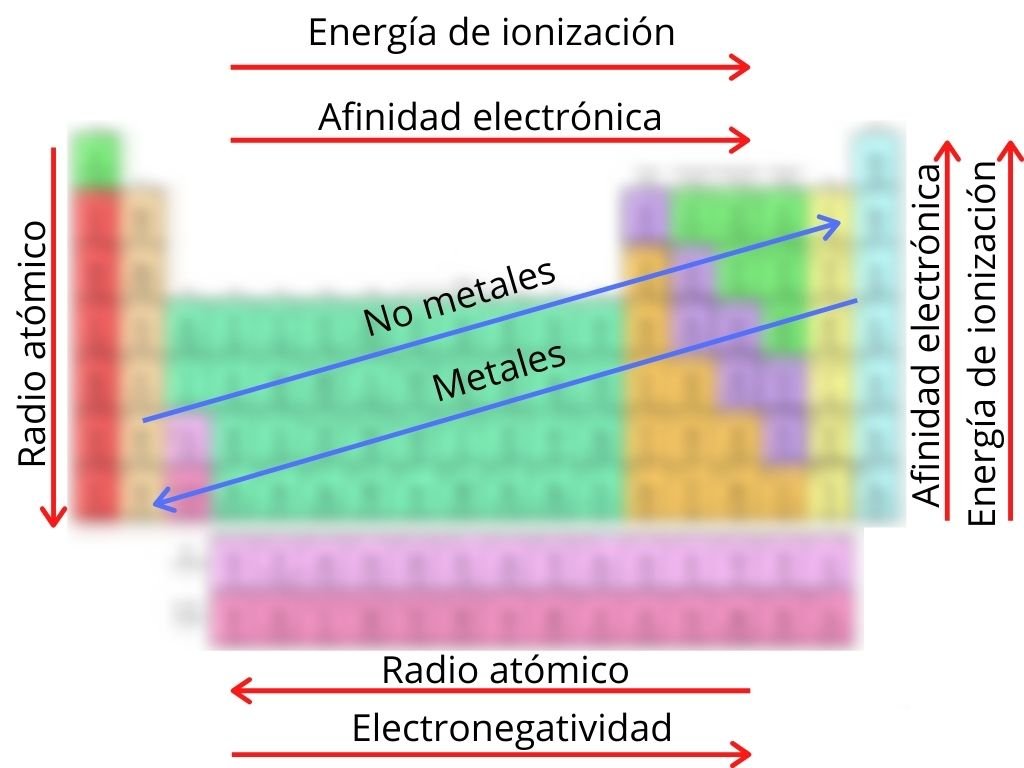
Electronegatividad energía de ionización afinidad electrónica radio atómico punto de fusión y. Las principales tendencias periódicas incluyen. Gráfico de tendencias de la tabla periódica.
Las tendencias periódicas más importantes en las propiedades atómicas se resumen en la Figura PageIndex 1. Radios atómicos e iónicos. En la tabla periódica se encuentra la más variada información como es el número atómico masa atómica valencia carácter metálico no metálico distribución electrónica.
Tendencias de la energía de ionización. Regla del octeto La regla del octeto enunciada en 1917 por Gilbert Newton Lewis dice que la tendencia de los iones de los elementos del sistema periódico es completar sus últimos niveles de energía con una cantidad de 8 iones que tienen carga negativa es decir electrones de tal forma que adquiere una configuración muy estable. Los metales alcalinotérreosberilio magnesio calcio estroncio bario.
Todos aquellos que tienen igual número de electrones en su último nivel presentan propiedades químicas similares correspondiendo el número de período en que se encuentra ubicado al del último nivel con electrones y el número de grupo guarda relación con la cantidad de electrones en la última capaLa tabla. Grupos Grupos tabla periódica En un grupo las propiedades químicas son muy similares porque todos los. Se reducen fácilmente son oxidantes.
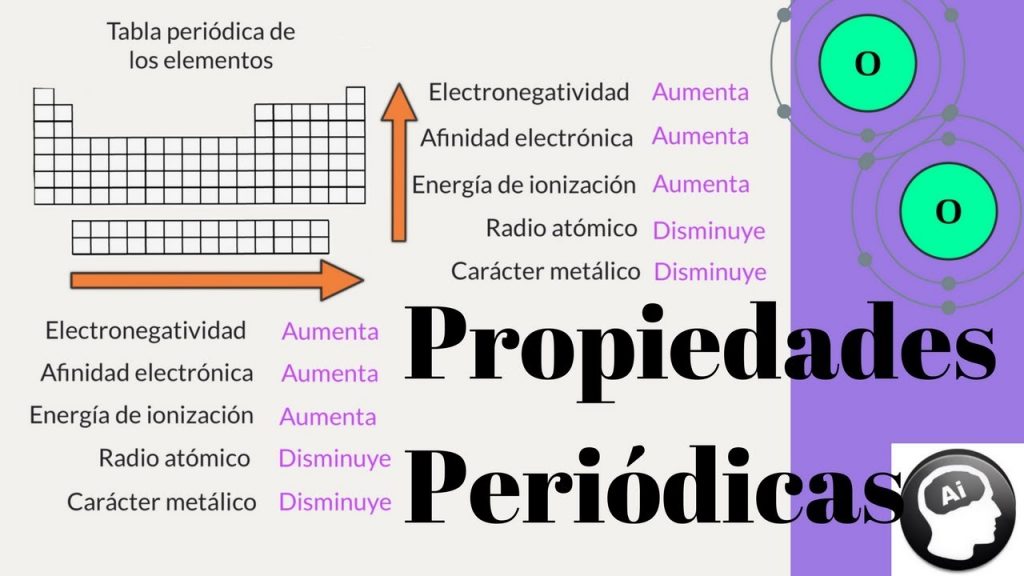
Las principales tendencias periódicas incluyen. Use esta tabla para ver de un vistazo las tendencias de la tabla periódica de electronegatividad energía de ionización radio atómico carácter metálico y afinidad electrónica. Metales de transición Tendencias del radio atómico en la tabla periódica.
La tendencia general para la afinidad electrónica es la de volverse más negativa al movernos a la derecha a lo largo de un periodo siendo los valores mayores los de los halógenos. Tendencia periódica de la energía de ionización. Variación de las propiedades periódicas radio atómico energía de ionización afinidad electrónica y electronegatividad 1 entrada Tabla Periódica.
Tienen tendencia a ganar electrones y formar iones negativos son muy electronegativos. Destaca una sola valencia.