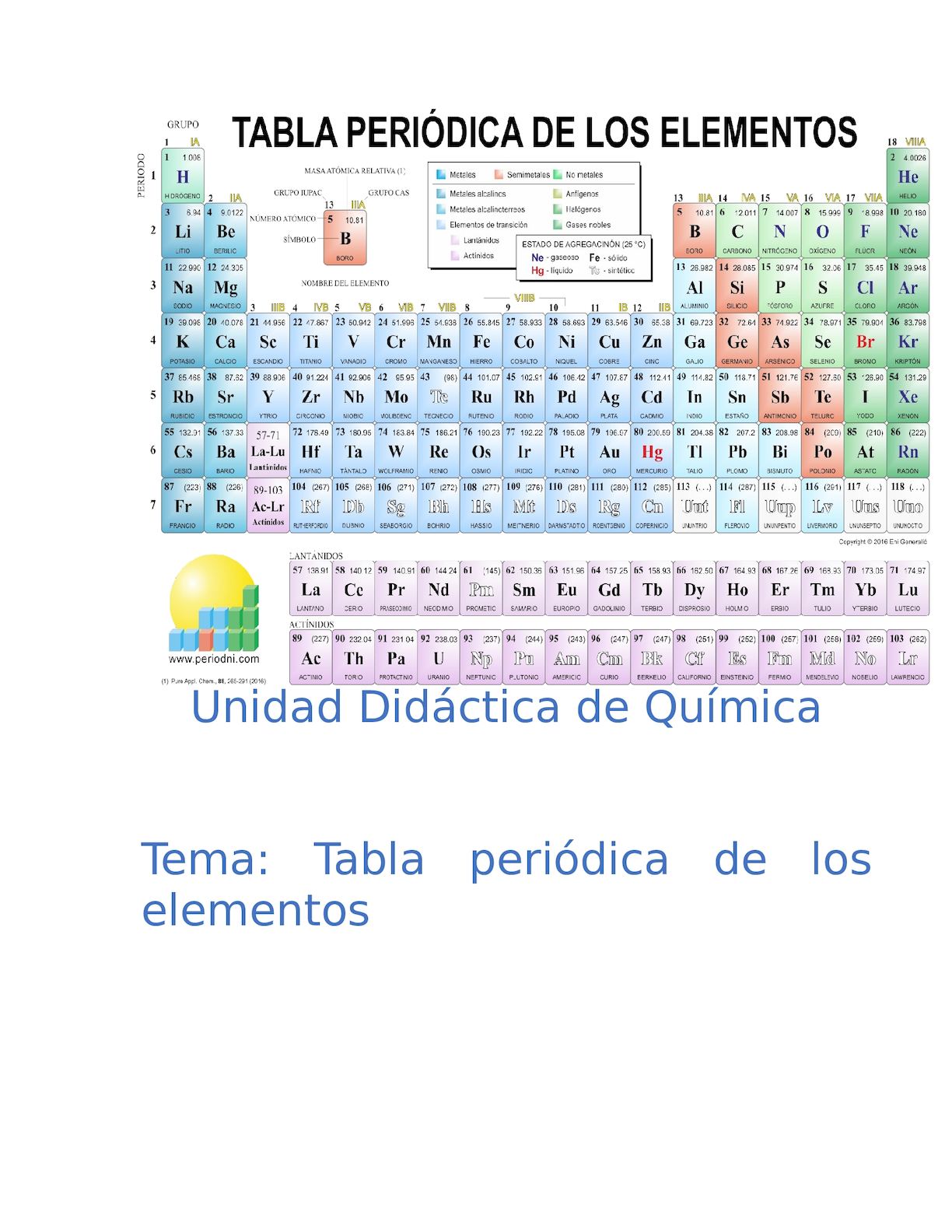
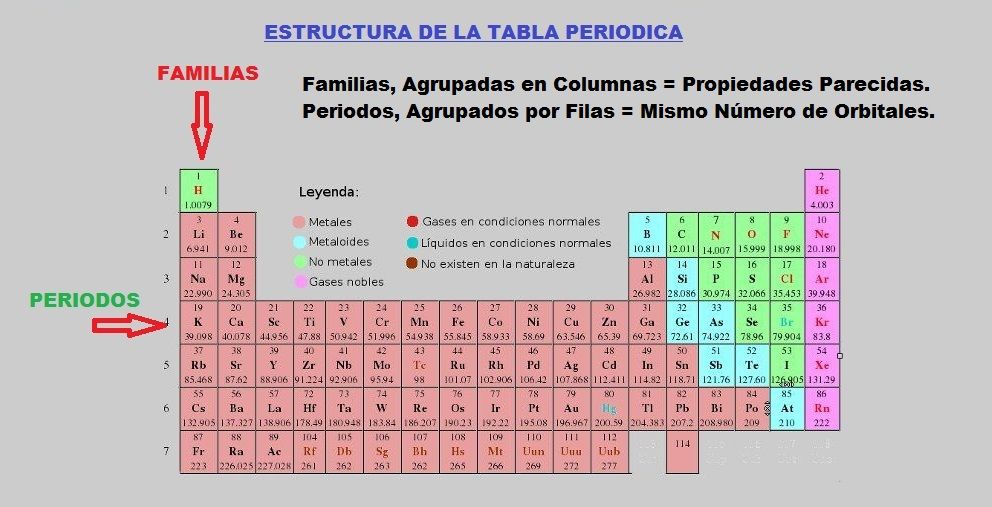
Propiedades Del Grupo 4a De La Tabla Periodica
2 La característica de este grupo es que tienen una configuración electrónica.
Propiedades del grupo 4a de la tabla periodica. Grupo 4a de la Tabla Periodica Los elementos de este grupo pueden considerarse como escasos en la corteza terrestre a excepción del silicio que tiene una abundancia natural de 2771 por ciento. Son por los siguientes elementos. O Aborto espontáneo o Perturbación del sistema nervioso.
Propiedades Quimicas De La Tabla Períodica. La familia del titanio pertenece a los metales de transición y está conformado por los elementos. En pequeñas cantidades el ion fluoruro previene la caries dental.
Carbono silicio germanio estaño y plomo. Grabado de vidrio tratamiento de la madera semiconductoresy en la fabricaciónde hidrocarburos fluorados. DIANA JARAMILLO INSTITUCIÓN EDUCATIVA EXALUMNAS DE LA PRESENTACIÓN IBAGUÉ - TOLIMA ÉNFASIS DE CIENCIAS GRADO.
O Disminución de las habilidades de aprendizaje de los niños. ELEMENTOS DE LA TABLA PERIODICA GRUPOS. Forma parte del grupo de los anfígenos en la tabla periódica y es un elemento no metálico altamente reactivo que forma fácilmente compuestos especialmente óxidos con la mayoría de elementos excepto con los gases nobles helio y neón.
Los metales alcalinotérreos son un grupo de elementos que se encuentran situados en el grupo 2 de la tabla periódica y son. O Perturbación en el comportamiento de. Estos elementos forman más de la cuarta parte de la corteza terrestre y solo podemos encontrar en forma natural al carbono al estaño y al plomo en forma de óxidos y sulfuros su configuración electrónica termina en ns2p2.
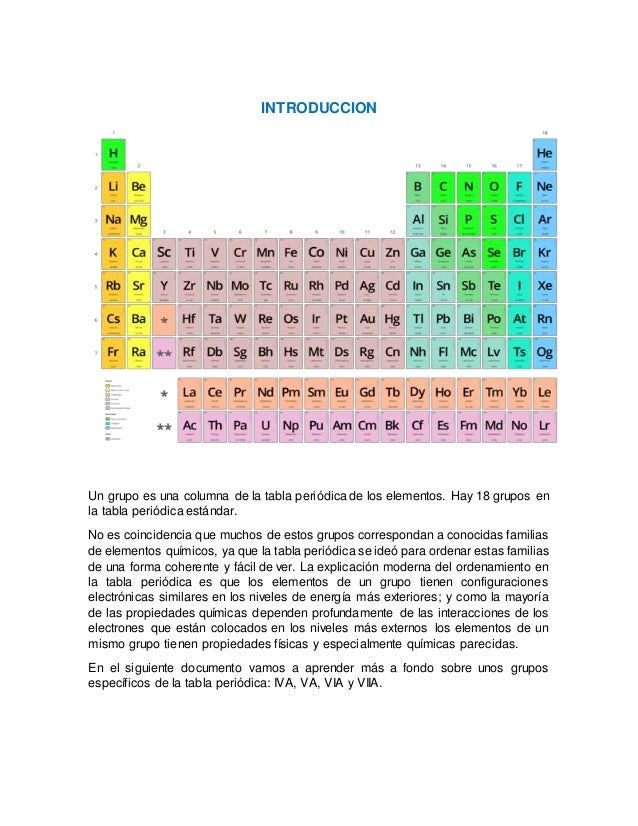
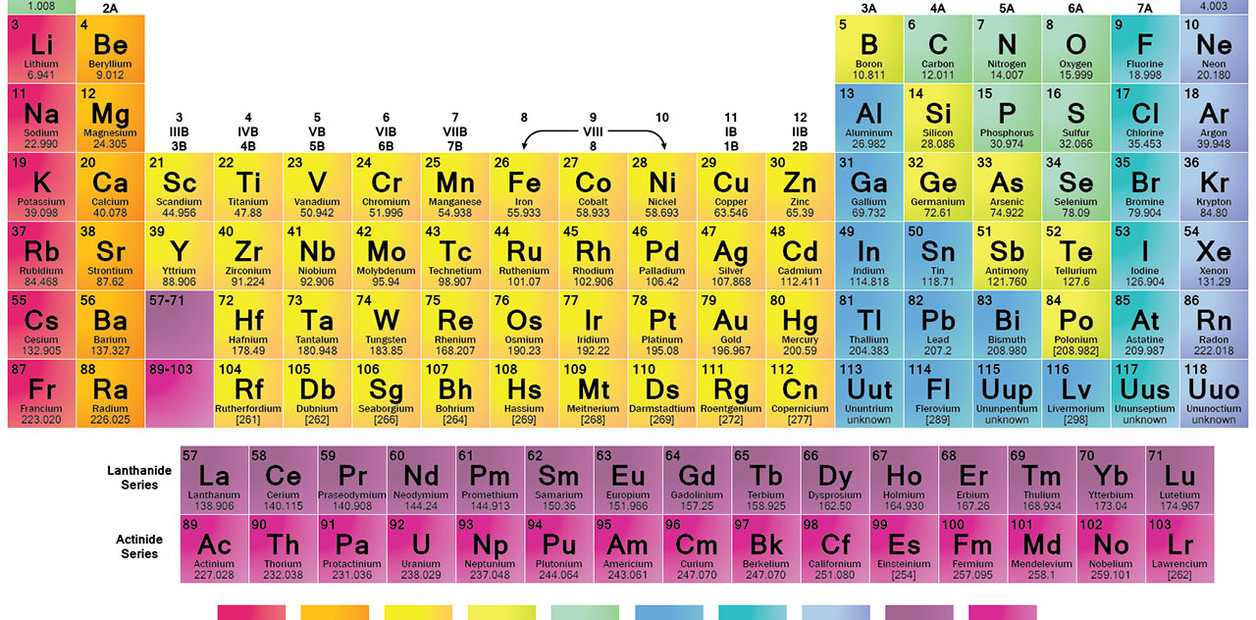
Es el grupo 14 o IV A de la tabla periódica de los elementos también conocido como grupo del carbono y está formado por los elementos. Enriquecimiento del isótopo fisionable 235 U mediante formación del hexafluoruro de uranio y posteriorseparaciónpor difusión gaseosa. Se requiere una gran cantidad de energía para romper estos enlaces durante la fusión o la vaporización por lo que el carbono tiene los puntos de fusión y de ebullición más altos de todo el grupo.
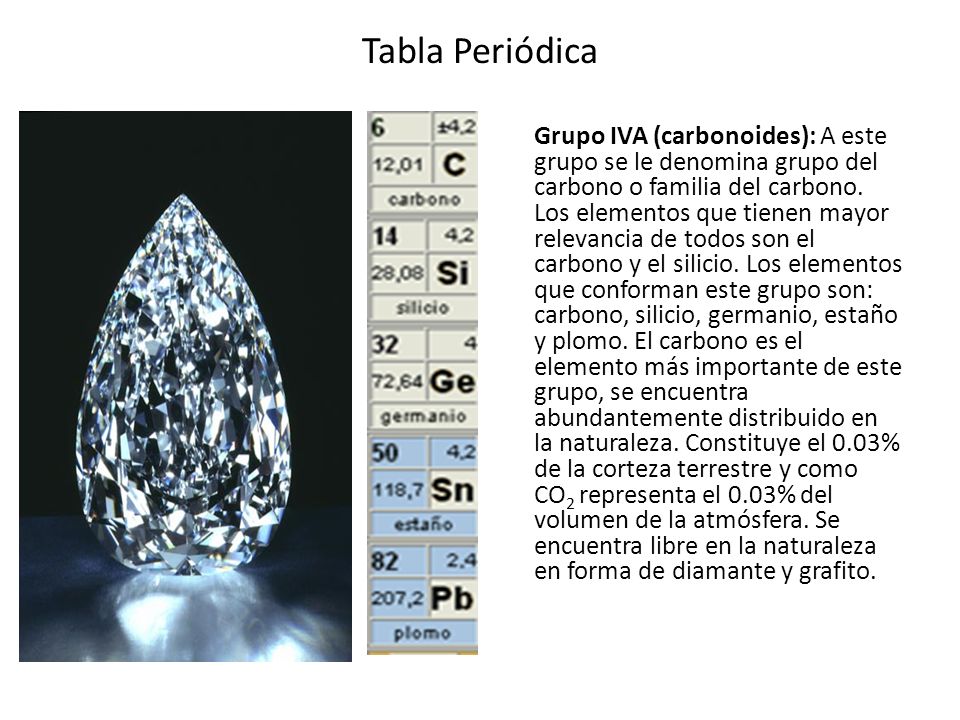
Carbono C Silicio Si Germanio Ge Estaño Sn Plomo Pb El carbono es un no metal es uno de los elementos mas significativos de la tabla periódica porque integra una gran cantidad de compuestos y entre ellos a las sustancias que forman a los seres vivos. MARÍA JOSÉ MELO CAICEDO PRESENTADO A. 8 Páginas 683 Visualizaciones.
El ácido fluorhídrico se emplea para. Carbono C silicio Si germanio Ge estaño Sn y plomo Pb. El carbono por ejemplo es un no metal típico y forma uniones covalentes.
Esta sustancia comprende una importante parte de la atmósfera y resulta necesaria para sostener la vida terrestre. LA FAMILIA DEL CARBONO. O Perturbación de la biosíntesis de hemoglobina y anemia.
República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación UE. Titanio Ti circonio Zr y hafnio Hf y rutherfordio Rf. 2 410 palabras Publicado.
GRUPO 4A Los elementos que componen a la familia del carbono o carbonoides son. Está situado en el grupo 14 de la tabla periódica de los elementos. Los elementos del grupo IVA son.
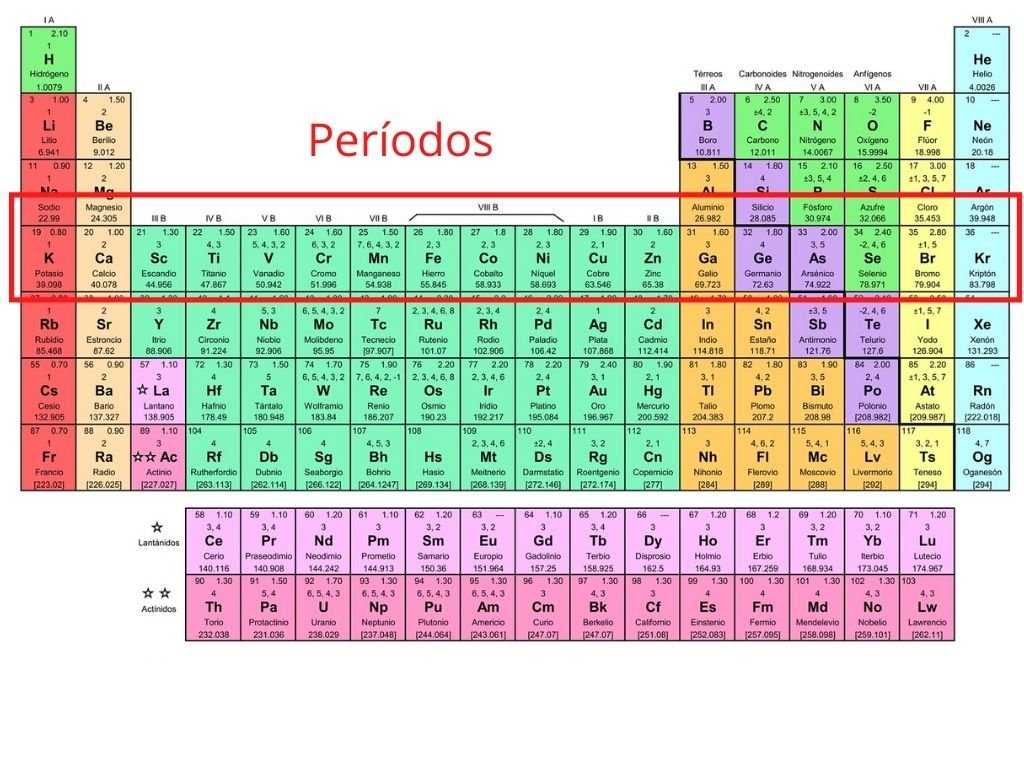
Grupo 4a de la tabla periodica. GRUPOS 4A 5A 6A Y 7A DE LA TABLA PERIÓDICA INTRODUCCIÓN En el siguiente documento se podrá encontrar toda la información sobre los grupos 456 y7 A de la tabla periódica con sus propiedades químicas su ubicación en la tabla periódica sus aplicaciones y algunos efectos ambientales que estos elementos químicos produces uno como metales y no metales. El silicio y el germanio son metaloides y el estaño y plomo son metales.
O Incremento de la presión sanguínea. El miembro más pesado del grupo el plo- Tabla 61 Propiedades de los elementos del grupo IVA. O Daño al cerebro o Distintos tipos de cáncer.
Estaño El estaño es un elemento químico de símbolo Sn del latín stannum y número atómico 50. Constituyen el grupo 14 de la Tabla Periódica. Forman másde la cuarta parte de la masa de la corteza.
7a 6a 5a y 4a PRESENTADO POR. Los elementos de este grupo son muy conocidos menos el germanio. Grupo 4 de la Tabla Periódica.
Se conocen 10 isótopos estables. Carbono C silicio si germanio ge estaño Snplomo Pb erristeneo Eo. 15 de agosto de 2010.
Este elemento se encuentra en la composición de muchas rocas. El berilio por ejemplo lo es muy poco y es debido a que los electrones del orbital 2s apantallan a cualquier electrón que quiera añadirse al orbital p mientras que el carbono tiene más afinidad electrónica de la que debería debido a que si gana un electrón tendrá el orbital 2p lleno hasta la mitad una configuración más estable de lo normal y eso hace que el átomo tenga más ganas de lo normal de ganar electrones la misma razón por la. O Disminución de la fertilidad del hombre a través del daño en el esperma.
Su principal mena es la casiterita. Todos los elementos de este grupo poseen el número de oxidación 3 exceptuando al galio indio y talio que tienen el grado de oxidación 1 pero el predomínate en galio e indio. Los elementos del Grupo IV A actualmente 14 tienen propiedades muy variables según su ubicación dentro del grupo.
El ion fluoruro facilita la formación de fluoroapatito Ca5PO43Fen lugar de. O Daño a los riñones.