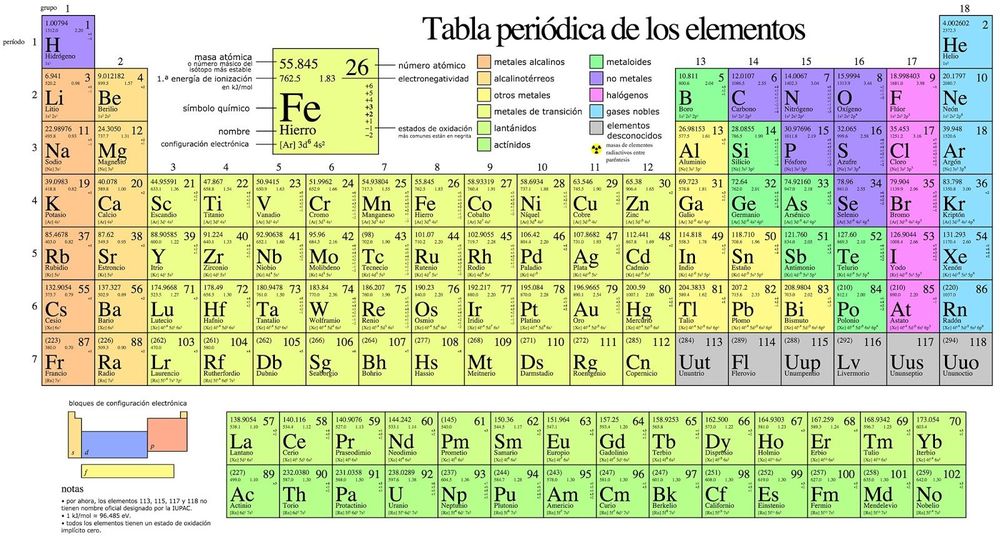
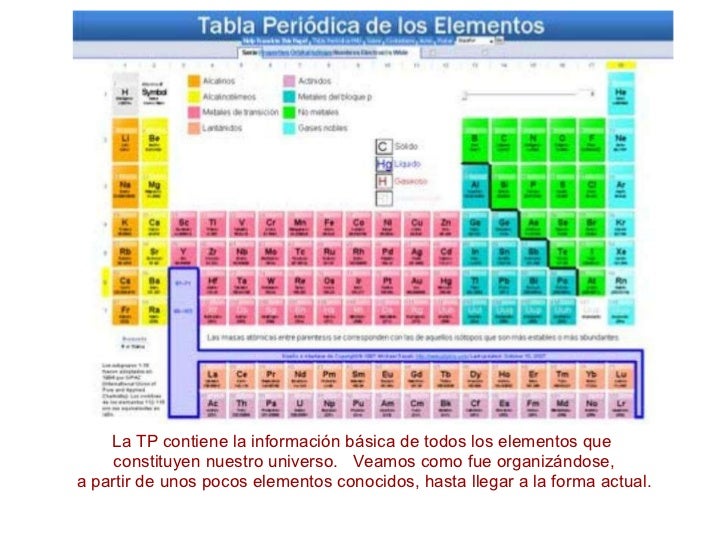
Aportaciones De Avogadro A La Tabla Periodica
-En 1803 formuló la teoría de que la materia está compuesta de átomos de diferentes masas que se combinan en proporciones sencillas para formar compuestos.
Aportaciones de avogadro a la tabla periodica. Aportaciones de meyer a la tabla periodica completa. Preparó en 1864 una tabla periódica de los elementos establecida según. Numéricas existentes entre los elementos químicos apoyándose en la teoría atómica de Dalton y la hipótesis de Avogadro.
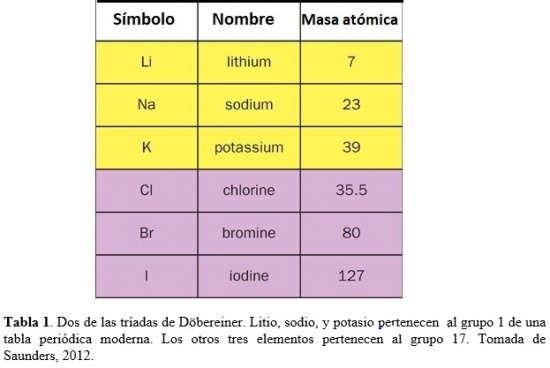
Sus masas atómicas y que señaló la ley de las octavas según la cual cada ocho elementos tienen propiedades similares. Avanzó en el estudio y desarrollo de la teoría atómica y en su honor se le dio el nombre al Número de Avogadro. APORTES A LA TABLA PERIODICA.
César Iván Nieves Arroyo Stanislao Cannizzaro Nació el 13 de julio de 1826 Palermo Italia Aportaciones a la tabla periódica y la química. En 1811 enunció el conocido principio o ley de Avogadro basado en la teoría atómica de John Dalton y la ley de Gay-Lussac sobre los vectores de movimiento en la. Este químico alcanzó a elaborar un informe que mostraba una relación entre la masa atómica de ciertos elementos y sus propiedades.
Avogadro contempló sorprendido cómo 1 litro de hidrógeno con 1 litro de gas cloro Formaban sólo 1 litro de gas Acido Clorhídrico y NO los 2 litros iniciales. 1898 fue un químico analítico inglés. Él destaca la existencia de similitudes entre elementosagrupados en.
A 150 años de su creación la Organización de las Naciones Unidas proclamó el 2019 como el Año Internacional de la Tabla Periódica como una forma de reconocer la función crucial que desempeñan las ciencias fundamentales especialmente la química y la física a la hora de aportar soluciones a muchos de los desafíos que afrontan los países miembros para aplicar la Agenda 2030 de. Que es masa. El estudio de los gases atrajo la atención del físico italiano Amadeo Avogadro que en 1811 formuló una importante ley que lleva su nombre.
Esta ley afirma que dos volúmenes iguales de gases diferentes contienen el mismo número de moléculas si sus condiciones de temperatura y presión son las mismas. En 1858 publicó una lista de pesos atómicos fijos que ahora se conocen como masas atómicas relativas para los sesenta elementos que. Otros Aportes Amedeo Avogadro se apoy en la teora atmica de John Dalton y en la ley de Gay-Lussac sobre los vectores de movimiento en la molcula y descubri que.
Aportaciones de Stanislao Cannizzaro ala tabla periodica. John Newlands 26 de noviembre de 1837 - 29 de julio de. Analizando los resultados experimentales conocidos en la época a la luz de la hipótesis de Avogadro hubiese llevado a la conclusión de que los elementos químicos gaseosos o fácilmente vaporizables conocidos en la época eran moléculas diatómicas H2 para el hidrógeno N2 para el nitrógeno O2 para el oxígeno Cl2 para el cloro Br2 para el bromo y I2 para el yodo.
Volmenes iguales de gases diferentes en las mismas condiciones de presin y temperatura contienen el mismo nmero de molculas. Llegó a establecer una clara distinción entre átomos y moléculas. La tabla periódica se descubrió gracias al químico italiano Stanislao Cannizzaro 1826-1910.
Amedeo Avogadro y sus aportaciones Numero de Avogadro Masa moecular Se entiende al número de entidades elementales de átomos electrones iones moléculas que existen en un mol de cualquier sustancia. Pensaba como Mendeleiev que su libro de texto debería estar basado en una clasificación de elementos y consiguió preparar. Sistema peri dico de los elementos.